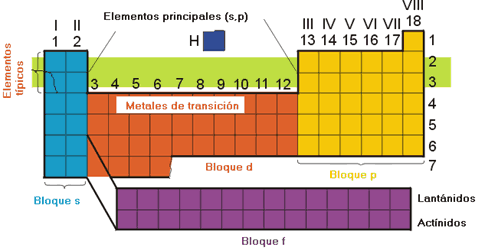
PROPIEDADES ATOMICAS Y SU VARIACION PERIODICA.
CARGA NUCLEAR EFECTIVA
Para explicar esta propiedad, consideremos el átomo de helio cuya configuración electrónica en estado fundamental es 1s2. Los dos protones del helio le confieren al núcleo una carga de +2, pero la fuerza total de atracción de esta carga sobre los dos electrones 1s es parcialmente balanceada por la repulsión entre los electrones. Como consecuencia, se dice que cada electrón 1s está protegido del núcleo por el otro electrón. La carga nuclear efectiva (Zefec), que es la que se ejerce sobre un electrón, se da por
Zefec = Z – σ
Donde Z es la carga nuclear real (es decir, el número atómico del elemento) y σ se llama constante de protección o constante pantalla. La constante pantalla es mayor que cero pero menor que Z.
Para ilustrar la protección de los electrones, analicemos lo siguiente: Se requiere de 2373KJ de energía para quitar el primer electrón de un mol de átomos de He y una energía de 5251kJ para quitar el segundo electrón; esta mayor energía se debe a que cuando queda un solo electrón no existe el efecto pantalla contra la carga nuclear +2.
En átomos con 3 o mas electrones, los niveles internos llenos protegen mejor a los electrones externos que los electrones del mismo nivel.

El concepto de carga nuclear efectiva permite entender los efectos de protección en las propiedades periódicas.
Para los elementos representativos, la carga nuclear efectiva aumenta de izquierda a derecha a lo largo de un período y de abajo hacia arriba en un grupo.
Así consideraremos que: � 
Variación de Z* en la tabla.
• Varía poco al aumentar Z en los e- de valencia de un mismo grupo, pues aunque hay una mayor carga nuclear también hay un mayor apantallamiento. Consideraremos que en la práctica cada e-de capa interior es capaz de contrarrestar el efecto de un protón.
Ejemplo:
Z* sobre el e- exterior del Li sería: 3 - 2 = 1, mientras que en el caso del Na sería: 11 -10 = 1, es decir apenas varía.
 Crece hacia la derecha en los elementos de un mismo periodo, debido al menor apantallamiento de los e- de la última capa y al mayor "Z", de manera que según se avanza en un periodo hacia la derecha crece más "Z" que "a", pues el apantallamiento de los e- de última capa es inferior a 1.
Crece hacia la derecha en los elementos de un mismo periodo, debido al menor apantallamiento de los e- de la última capa y al mayor "Z", de manera que según se avanza en un periodo hacia la derecha crece más "Z" que "a", pues el apantallamiento de los e- de última capa es inferior a 1.
Ejemplo:
Z* sobre uno de los e- exteriores del Be sería: 4 - (2 + 0,8) = 1,2 mientras que en el caso del Li era: 3 -2 = 1. Nota: el valor 0,8 de apantallamiento del e- de la segunda capa es orientativo; lo importante es que es un número inferior a 1.
Carga nuclear efectiva y reactividad.
La atracción que sufren los electrones de valencia no sólo dependen de la carga nuclear efectiva, sino también de la distancia del e- al núcleo (ley de Coulomb). Por ello, la reactividad de los átomos dependerá de ambos factores.
Así, los metales serán tanto más reactivos cuanto menor Z* y mayor distancia al núcleo, es decir, cuando pierdan los e-con mayor facilidad.
Ejemplo: El e- 4s del K es más reactivo que el 3s del Na.
|
Aumento en la Reactividad
|

Sin embargo, los no-metales serán más reactivos a mayor Z* y menor distancia al núcleo, es decir, cuando los e- que entran sean más atraídos.
Ejemplo: El e- que capture el F será más atraído que el que capture el O o el Cl.
TAMAÑO ATÓMICO
El radio atómico es la distancia que existe entre el núcleo y la capa de valencia. Por medio del radio atómico es posible determinarse el tamaño del átomo. Se define como: "la mitad de la distancia de dos átomos iguales que están enlazados entre sí".
Por dicha razón, se habla de radio covalente y de radio metálico según sea el tipo de enlace por el que están unidos. Es decir, el radio de un mismo átomo depende del tipo de enlace que forme, e incluso del tipo de red cristalina que formen los metales
Existen técnicas que permiten calcular el tamaño de un átomo, en primera instancia a los elementos metálicos que poseen una estructura muy variada, sus átomos se encuentran enlazados uno con el otro formando una red tridimensional.
Los átomos atómicos están determinados en gran medida por la fuerza de atracción del núcleo hacia los electrones. A mayor carga nuclear efectiva, los electrones estarán más fuertemente enlazados al núcleo y menor será el radio atómico y a medida que desciende en un grupo, se encuentra que el radio atómico aumenta, conforme aumenta el número atómico.

Elradio atómico A) En un metal;
B)En una molécula diatómica.

En la tabla periódica, si esta de izquierda a derecha disminuye el número atómico y de arriba hacia abajo aumenta su número atómico.
El radioatómico en la Tabla Periódica.

Radio iónico
Es el radio que tiene un átomo cuando ha perdido o ganado electrones, adquiriendo la estructura electrónica del gas noble más cercano.
Los cationes son menores que los átomos neutros por la mayor carga nuclear efectiva (menor apantallamiento o repulsión electrónica). Cuanto mayor sea la carga, menor será el ion; así, en un mismo periodo, los metales alcalinotérreos serán menores que los alcalinos correspondientes, dado que en ambos casos existe el mismo apantallamiento, mientras que los alcalinotérreos superan en una unidad la carga nuclear de los alcalinos.
Los aniones son mayores que los átomos neutros por la disminución de la carga nuclear efectiva (mayor apantallamiento o repulsión electrónica). Cuanto mayor sea la carga, mayor será el Ion; así, en un mismo periodo, los anfígenos serán mayores que los halógenos correspondientes, dado que en ambos casos existe el mismo apantallamiento, mientras que los halógenos superan en una unidad la carga nuclear de los anfígenos.
En general, entre los iones con igual número de electrones (isoelectrónicos) tiene mayor radio el de menor número atómico, pues la fuerza atractiva del núcleo es menor al ser menor su carga.
COMPARACIÓN DE TAMAÑOS DE ATOMOS E IONES
Metales alcalinos Halógenos Iones isolectrónicos

ENERGÍA DE IONIZACIÓN
La energía de ionización es la mínima energía requerida para quitar un electrón de un átomo gaseoso en su estado fundamental.
La formación de los compuestos y moléculas no solo depende de la existencia de los niveles de energía en los elementos. Si no también de la energía de ionización de átomos involucrados,
La energía de ionización de un átomo es la cantidad de energía que se requiere para desalojar del átomo al electrón ligado más débilmente. En este proceso el átomo adquiere una carga positiva, y se le denomina catión.
En la Tabla Periódica, la energía de ionización aumenta en un período según aumenta el número atómico (de izquierda a derecha) y en un grupo disminuye a medida que aumenta su número atómico (de arriba hacia abajo).
LaEnergía de Ionización en la tabla Periódica
La energía de ionización mide la facilidad con que un átomo cede un
Electrón; se mide en kilo joules/ mol (kJ/mol).

AFINIDAD ELECTRÓNICA
La afinidad electrónica es la cantidad de energía desprendida cuando un átomo gana un electrón adicional. En ese proceso el átomo queda con carga negativa y recibe el nombre de anión.
Es otra propiedad de los átomos que influye en su comportamiento químico es su habilidad para aceptar uno o más electrones, la cual se conoce como afinidad electrónica.
Esta propiedad determina cuál es el cambio de energía cuando un átomo acepta un electrón en el estado gaseoso, y guarda una íntima relación con la energía de ionización. Mientras más negativa sea la afinidad electrónica, mayor será la tendencia del átomo a aceptar un electrón.

La tendencia del átomo a aceptar electrones aumenta al desplazarse de izquierda a derecha en un periodo.
La afinidad electrónica de los no metales es mayor (más negativo) comparada con la de los metales y, en comparación con los elementos próximos a los gases nobles (menos negativos), es sensiblemente más grande.
De esta forma se representa: la afinidad electrónica. En la tabla periódica:
NUMERO DE OXIDACION
El número de oxidación es un número entero que representa el número de electrones que un átomo pone en juego cuando forma un compuesto determinado. El numero será positivo cuando tenga la capacidad de cederlos a otro átomo, de lo contrario será negativo es decir cuando gane electrones
LAS REGLAS CONVENCIONALES PARA LA DETERMINACIóN DEL NúMERO DE OXIDACION
1. El número de oxidación de un elemento libre es cero, ya sea monoatómica o poliatómica. Ejemplo Al0, Fe0, Cl20, l20.
2. El número de oxidación de todos los elementos del 1A es +1. Ejemplo: Li+1, Na+1, K+1, etc.
3. El número de oxidación de todos los elementos del grupo 2A es +2. ejemplo Be+2, Mg+2, Ca+2, Sr+2.
4. El número de oxidación de los hidrógenos es +1, cuando forma compuestos, en los hidruros es -1.
5. En el oxígeno el número de oxidación es -2, cuando forma compuestos y no en peróxidos que trabaja con -1.
6. Halógenos, formando sales: -1. F-1, Cl-1, K-1, I-1.
7. Sumatoria del número de oxidación en una molécula es cero.
+1 +4 -2
H2 C O3
+2 +4 -6= 0
8. Número de oxidación en un ión poliatómico es igual a la carga del ión.
+5 -2
P O4 -3
+5 -8 = -3
ELECTRONEGATIVIDAD
La electronegatividad es una medida de la fuerza de atracción que ejerce un átomo sobre los electrones de otro en un enlace covalente. Los diferentes valores de electronegatividad se clasifican según diferentes escalas, entre ellas la escala de Pauling y la escala de Mulliken.
En general, los diferentes valores de electronegatividad de los átomos determinan el tipo de enlace que se formará en la molécula que los combina. Así, según la diferencia entre las electronegatividades de éstos se puede determinar (convencionalmente) si el enlace será, según la escala de Pauling:
Iónico (diferencia superior o igual a 2)
Covalente polar (diferencia entre 2 y 0.4)
Covalente no polar (diferencia inferior a 0.4)
Mientras más pequeño es el radio atómico, mayor es la energía de ionización y mayor la electronegatividad.
Escala de Pauling
La escala de Pauling es una clasificación de la electronegatividad de los átomos. En ella, el elemento más electronegativo (Flúor), tiene un índice de 4.0, mientras que el menos electronegativo (Francio) lleva un valor de 0.7. Los demás átomos llevan asignados valores intermedios.
Globalmente, puede decirse que la electronegatividad aumenta de izquierda a derecha en la Tabla Periódica de los Elementos, y que decae hacia abajo. De esta manera los elementos de fuerte electronegatividad están en la esquina superior derecha de la tabla.
LA ESTEQUIOMETRIA
La composición centesimal: indica el porcentaje en masa, de cada elemento que forma parte de un compuesto. Se obtiene por análisis gravimétrico y conociendo los pesos atómicos de los compuestos puede determinarse su fórmula mínima o molecular. También se obtiene a partir de la fórmula molecular del compuesto, ya que ésta nos indica el número de átomos de cada elemento presentes en el compuesto. Forma parte de los cálculos estequiométricos, y fue de gran importancia en la Historia de la química para la determinación de los pesos atómicos y moleculares, por ejemplo los trabajos de Berzelius y Cannizzaro.
¿Como podemos deducir formula química de un compuesto, apartir del dibujo del cristal o molécula?
He visto dibujos o exquemas de cristales y moléculas químicas representadas o dibujadas en el papel, junto con su fórmula química. Pero si no tuviésemos la formula escrita al lado, ¿sería posible deducirla apartir del dibujo del cristal o molécula? ¿Cómo podríamos calcular la electronegatividad de a celda unidad del cristal o molécula? ¿Sería diferente o más complicado si esta posee enlaces secillos y dobles, o sencillos y triples, como he visto en algunas? Por ahí he visto también casos extraños de un números de valencia elevados, que no tienen adjudicados los elementos químicos en la Tabla periódica. Creo que le llaman número de valencia, no convencional ¿Por que se forman estos números de valencia tan elevados, en cristales metálicos? ¿En moléculas también ocurrre? ¿Tendrían valores de electronegatividad muy elevados a causa de esto numeros de valencia tan altos? También he visto cristales raros por ahí, como los de beta-tugsteno, que en lugar de tener un único átomo, centrado en las caras, son dos ¿Podría suceder que otras variantes, pudiesen contener un mayor número de átomos centrados en las caras, como 3 ó 4? ¿Que ejemplos tendríamos? ¿Por que se forman estas fases o cristales no convencionales? En la esructura hexagonal, metálica, he visto que pueden estar centradas en el cuerpo por tres átomos, formando un triángulo, pero no he visto nada parecido en estructuras cúbicas, centradas en el cuerpo y en las caras. Un caso curioso y que me ha llegado a sorprender más, es el de la estructura del azul prusia, con átomos de Fe2 y Fe3. es más complejo que la de perovskita, con átomos centrados en los vértices del cubo. Conteniendo el Azul Prusia parejas de átomos unidos con enlace riple, unidos a los átomos de los águlos, con enlaces sencillo, son 24 átomos. Creía que no podía haber nada más complejo que las estructuras de perovskitas; pero parece que si lo hay, al menos el Azul prusia lo es, lo cual es increible!. Cuando estudiaba en el Instituto, no vimos nada parecido, cuando estudiabamos las estructuras cristalina en Tecnología y en la asignatura de Geología (tampoco lo de las valencias no convencionales, en estas dos) ¿Y después de esto hay más complejo todavía?. Creía además, que las formas cristalinas, compuestas por un elevado número de átomos, serían inestables, a presión y temperatura ambiente. Como ocurre con el azufre elástico que forman ciclos de 20 átomos, de tipo benceno, C6H6; pero sólo son estables a temperaturas o presiones muy elevadas, no siendo posible observarlo en condiciones ordinarias de p-T, a 20ºC y 1atm. de presión.